Sammanfattning
I en uppmärksammad artikel skriver Smith-Bindman et al. (JAMA 2025) att ett års CT-användning i USA beräknas orsaka ca 100 000 framtida fall av cancer. Om nuvarande praxis består skulle detta innebära att 5% av framtida årliga cancerdiagnoser beror på CT-exponering.
Beräkningen bygger på riskmodeller, vilket bidrar till betydande osäkerhet; resultatet bör därför inte bokstavstolkas. Studien är dock välgjord och med dagens data framstår det som svårt att göra en väsentligt bättre uppskattning (mer om detta i fördjupningen nedan).
Smith-Bindman et al. är inte den första artikeln i sitt slag: Brenner och Hall (2007) samt Berrington de González et al. (2009) uppskattade andelen strålningsinducerade cancerfall från CT-undersökningar till 1,5–2% respektive 1–3%.
De främsta skillnaderna mellan Smith-Bindman et al. och dessa tidigare studier är att CT-användningen i USA ökat med över 30%[1] sedan dess, samt att Smith-Bindman använder en bättre metod för att uppskatta organdoser från CT-undersökningar som tar hänsyn till kroppsstorlek och multipla scans (vilket möjliggjorts av den utveckling som skett inom insamling av metadata från röntgenundersökningar).
I Sverige är både CT-användningen och dosnivåerna betydligt lägre än i USA. KcRN har därför räknat om Smith-Bindmans resultat till svenska förhållanden baserat på CT-statistik från SSM samt en egen insamling av CT-metadata från 15 sjukhus i landet (se fördjupning nedan). Omräkningen landar på 1,3% av framtida cancerdiagnoser, vilket främst förklaras av 40% färre CT-undersökningar samt omkring 50% lägre förmodad risk per undersökning, kopplat till 20–70% lägre organdoser för olika kroppsdelar.
CT har uppenbart stor nytta för patienter och sjukvården, och ofta är risken med att inte göra en undersökning större än risken från strålningen. En betydande andel av undersökningar är dock inte berättigade. I en SSM-rapport från 2009 bedömdes ca 20% av CT-undersökningar i Sverige vara oberättigade, och 2012 uttryckte de nordiska strålsäkerhetsmyndigheterna en oro över den stora ökningen av CT-användning. Smith-Bindman et al. är därför en viktig påminnelse om värdet av berättigandebedömningar och stråldosoptimering.
Fördjupning för den mer intresserade läsaren
Metod och resultat i Smith-Bindman et al.
Kortfattat kan metoden beskrivas som bestående av fyra delar:
- Enkätdata från 235 sjukhus samt 78 röntgenanläggningar används för att uppskatta den totala CT-användningen i USA, inklusive ålders- och könsfördelning.
- En databas med metadata från CT-undersökningar från 143 sjukhus används för att uppskatta frekvensen av specifika undersökningstyper, inklusive exponeringsparametrar och patientegenskaper (ålder och storlek på bestrålad kroppsdel). Baserat på detta gjordes en indelning i 418 representativa grupper för olika CT-kategorier, åldersgrupper och kön.
- Medelorgandoser till varje grupp beräknades, baserat på de undersökningsspecifika exponeringsparametrarna, via Monte Carlo-simuleringar i storleksmatchade beräkningsfantom.
- Cancerrisk från dessa organdoser beräknades därefter via ett program baserat på riskmodeller från BEIR-VII. Detta tar hänsyn till ålder vid exponering och använder livslängdstabeller för en amerikansk befolkning.
Totalt utfördes 93 miljoner undersökningar på 62 miljoner patienter under ett år. De undersökningsområde som stod för flest beräknade inducerade cancerfall var som väntat buk följt av thorax. Ett intressant resultat är att om vi tittar på åldersfördelningen så var bidraget till det totala antalet cancerfall ganska jämnt fördelat mellan patienter undersökta från 18–29 års ålder upp till 60–69 år för att sedan halveras vid 70–79 år och därefter bli försumbart vid >80 år. Den vanligaste cancertypen var lungcancer följt av en relativt jämn spridning av cancer i diverse bukorgan, bröstcancer samt leukemi. För barn var sköldkörtelcancer vanligast, följt av lung- och bröstcancer.
Styrkor och svagheter i Smith-Bindman et al.
Smith-Bindman och medförfattare Amy Berrington de González är båda välkända namn inom området, med lång erfarenhet av liknande register- och databasbaserade studier. Berrington de González är också en av huvudpersonerna bakom det verktyg (RadRAT) som används för beräkningen av cancerrisk. Medförfattare Wesley Bolch är ett framstående namn inom dosimetri och har varit med och utvecklat den metod som används för att beräkna organdoserna i studien.
Hantverket håller därför som väntat en till synes hög nivå. Datamaterialet framstår som bra, med en rimlig och tillräckligt finkornig uppdelning i CT-kategorier och åldersgrupper för att göra en bra uppskattning av de genomsnittliga organdoserna i populationen. En viktig faktor för noggrannheten i dosimetrin är det faktum att metadatan innehåller effektiv diameter för den skannade kroppsdelen (beräknad från bildtagningen), vilket möjliggör storleksmatchning med de 370 olika antropomorfiska beräkningsfantomen. Användandet av metadata möjliggör också summering av organdoser för undersökningar med multipla[2] scans (29%). Sammantaget är det svårt att se att metoden för dosuppskattningen skulle kunna göras väsentligt mycket bättre.
Även vad gäller beräkning av cancerrisker är det svårt att se att det skulle finnas en signifikant bättre metod än BEIR VII:s riskmodeller så som de implementerats i RadRAT. Alla riskmodeller är som bekant förknippade med stora osäkerheter vid låga stråldoser (<100 mGy). I detta fall är dock exponeringen både akut och inte extremt låg (typiskt ca 25 mGy för bukorgan och 50 mGy för skalle) vilket gör extrapoleringen mindre långtgående än i många andra studier. Förmodligen står ändå riskmodellerna för det enskilt största bidraget till osäkerhet i deras slutsats.
Ett stort och viktigt frågetecken i studien är att personer som undersöks med CT tillhör en selekterad grupp som antingen är/misstänks/har varit sjuka eller skadade. Den förväntade livslängden (på gruppnivå) är därför rimligen kortare än i normalbefolkningen. Men eftersom cancerprojektionerna använder livslängdstabeller för normalbefolkningen skulle det leda till en överskattning av antalet cancerfall (det kan också finnas vissa skillnader mellan gruppernas cancerrisk pga miljö- och genfaktorer, vilket faller utanför ramen för denna artikel). Smith-Bindman et al. adresserar detta genom att exkludera den andel av undersökningarna (10,6%) där patienten förväntas dö inom ett år. Detta framstår spontant som för kort och inte heller förenligt med deras användning av en latenstid på 4–11 år för solida cancrar vilket står för majoriteten av fallen. Tyvärr innehåller artikeln och referenserna varken en motivering, data eller diskussion kring detta. Är exklusionen som Smith-Bindman gjort tillräckligt stor för att undvika bias pga överdödligheten bland CT-undersökta patienter? Leder användandet av livslängdstabeller för normalbefolkningen till en stor överskattning av beräknade cancerfall?
En första ledtråd kan vi hitta i känslighetsanalysen i det supplementära materialet till Smith-Bindmans artikel. Enligt denna skulle antalet uppskattade cancerfall bara sjunka med 2,6% om Smith-Bindman utökat exkluderingen till två år.
En andra ledtråd kan vi hitta i Berrington de González et al. (2009). Här exkluderades den andel som inte förväntades överleva 5 år (11%) samt undersökningar som var associerade med cancerdiagnoser (9%). Man kan fråga sig huruvida det är rätt att exkludera samtliga patienter med cancerdiagnos; men om Smith-Bindman exkluderat motsvarande andel som Berrington de González hade resultatet bara blivit något lägre.
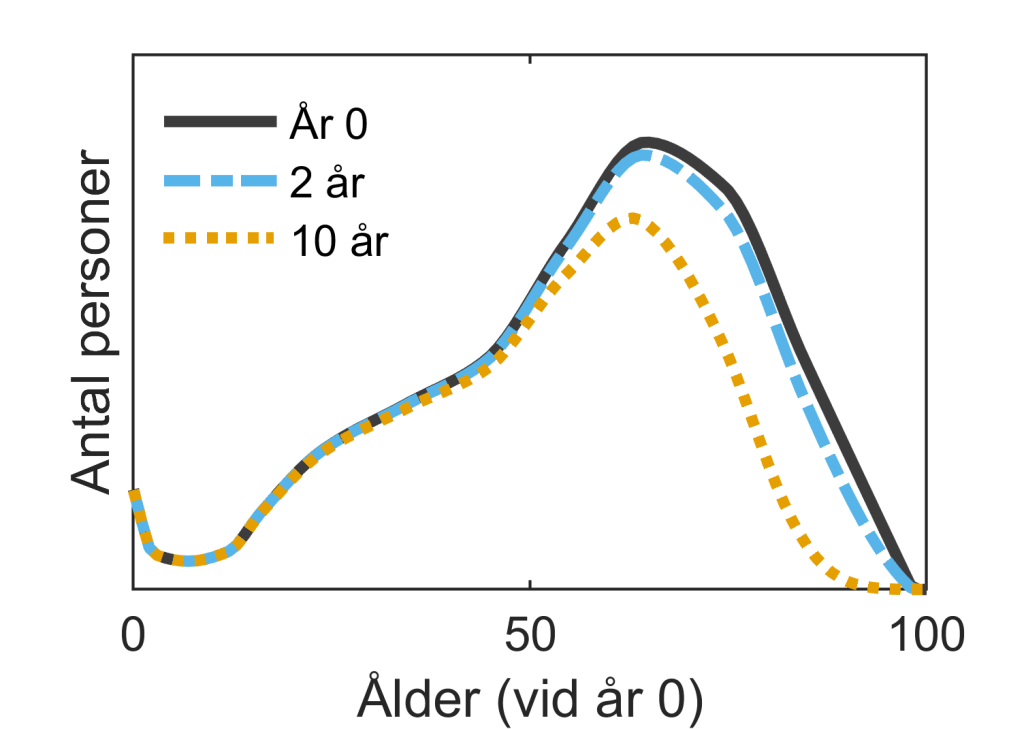
En tredje ledtråd kan vi få via Mataac et al. (2024), den möjligen enda studie hittills som publicerat överlevnadsdata för allmänna CT-undersökningar (37 000 patienter; tyvärr bara från ett sjukhus). Här ser vi att dödligheten är hög under första och andra året, för att därefter plana ut. För de mindre grupper som genomgått många undersökningar var dödligheten mycket hög: i gruppen med högst kumulerad dos (≥100 mSv) var bara 50% vid liv efter 2 år samt 37% efter 10 år (Mataac grupperar tyvärr patienterna efter stråldos snarare än antal undersökningar; ≥100 mSv borde motsvara ungefär ≥5 undersökningar). Om vi slår ihop de olika dosgrupperna i studien får vi en överlevnad för hela kohorten på 85% vid 2 år respektive 75% vid 10 år. För att jämföra detta med Smith-Bindmans metod vill vi veta vad överlevnaden skulle ha varit för normalpersoner, vilket Mataac et al. inte anger. Vi kan dock själva göra en grov uppskattning av detta genom att applicera en amerikansk livslängdstabell på Smith-Bindmans åldersdistribution (Figur 1), vilket då ger en överlevnad på 95% vid 2 år respektive 78% vid 10 år. Slutsatsen av denna jämförelse är alltså att överlevnaden för en CT-population är mycket lägre än normalt de första åren, men att den efter 10 år inte verkar[3] vara avsevärt mycket lägre än förväntat för normalpersoner.
Sammantaget tyder dessa tre jämförelser på att Smith-Bindmans exklusion nog är tillräckligt stor. Och att resultatet åtminstone inte är kraftigt överskattat på grund av den högre dödligheten hos CT-patienter.
Omräkning till Sverige
Som underlag för en jämförelse har KcRN samlat in CT-metadata från ett antal platser i landet. Totalt 325 000 undersökningar från sammanlagt 15 sjukhus i Skåne, Västra Götaland, Stockholm och Dalarna (inom 2024–2025). Om vi tillåter oss vissa antaganden och förenklade korrektioner så kan Smith-Bindmans uppskattade 5% av framtida cancerfall räknas om till en motsvarande siffra för Sverige.
- Skillnad i antal undersökningar
Smith-Bindman et al. rapporterar 93 miljoner undersökningar år 2023, vilket motsvarar ca 0,28 per capita/år. I SSM 2025:07 uppskattas antalet CT-undersökningar till 168 per 1000 invånare, vilket motsvarar 0,17 per capita/år. Detta ger en kvot mellan Sverige och USA på 0,61 (dvs ca 40% färre undersökningar per capita i Sverige).
Korrektionsfaktor#us (USA→Sverige): 0,61 - Skillnad i stråldoser
Smith-Bindman rapporterar CT-protokoll-specifika organdoser för åldrarna 50–59 i det supplementära materialet. Från detta beräknades ett viktat[4] medelvärde för de organ som förväntas befinna sig inom undersökningsområdet för fyra representativa kategorier: buk, skalle, thorax, ryggrad (vilka tillsammans står för 85% av beräknade cancerfall).
För det svenska datamaterialet selekterades åldrarna 50–59 år, och det storleksanpassade dosmåttet (SSDE) användes som estimat av medelorgandos i undersökningsområdet. SSDE summerades i de fall då flera serier körts av samma kroppsdel. Doserna räknades separat för regionerna och medelvärdesbildades för att ge lika vikt.
Detta gav uppskattade medelorgandoser (per hel undersökning) för kategori buk/skalle/thorax/ryggrad på 25/53/25/46 mGy för USA respektive 12/42/10/14 mGy för Sverige, dvs 20–70% lägre i Sverige. Fördelningen mellan de fyra kategorierna (antal undersökningar) var förhållandevis likvärdig[5] i de båda materialen.
En slutlig korrektionsfaktor för skillnaden mellan länderna erhölls därefter genom att ta hänsyn till respektive kategoris relativa bidrag till beräknat antal cancerfall. Detta gav en kvot mellan Sverige och USA på 0,47 (dvs 53% lägre cancerrisk per undersökning i Sverige om vi ignorerar övriga skillnader mellan populationerna).
Korrektionsfaktorstråldos (USA→Sverige): 0,47
- Skillnad i åldersfördelning
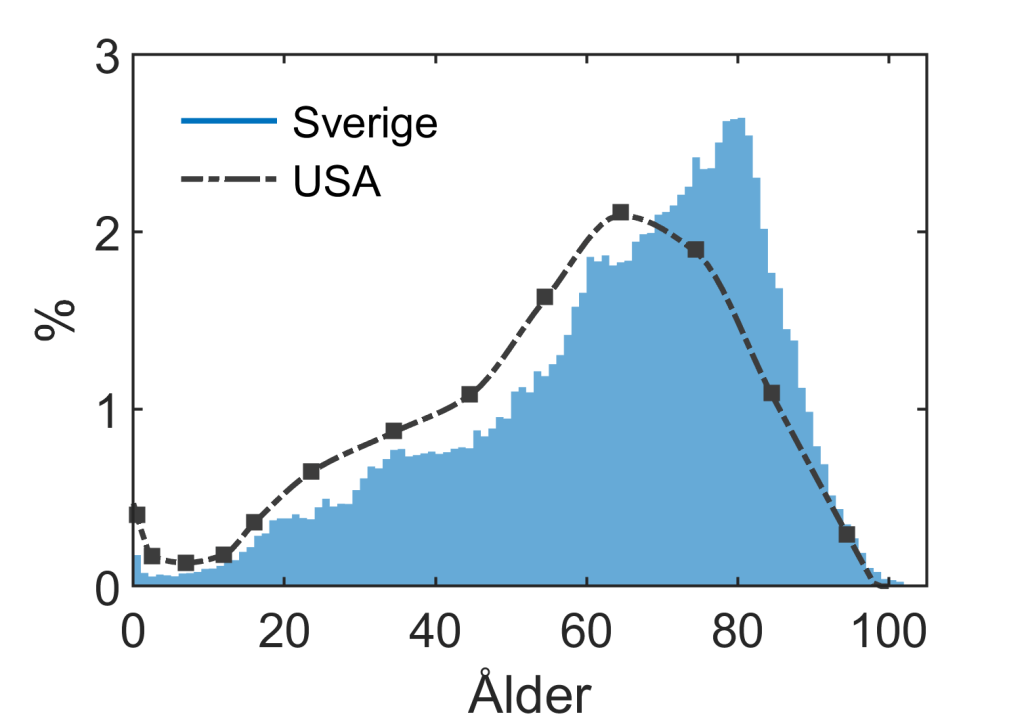
Det svenska stickprovet har en högre genomsnittsålder och färre antal barn och unga jämfört med USA (se Figur 2 nedan). Svenska patienter var i medel ca 5 år äldre vid exponering.
Högre ålder vid exponering innebär en lägre livstidsrisk för cancer (om USA haft Sveriges åldersfördelning vid exponering skulle effekten vara ca 20% färre förväntade cancerfall). Samtidigt är också den förväntade livslängden högre i Sverige vilket omvänt ökar antalet förväntade cancerfall. En överslagsberäkning visar att dessa två effekter mestadels tar ut varandra.[6]
Korrektionsfaktorålder (USA→Sverige): ≈ 1
- Skillnad i cancerincidens
Skillnaden mellan Sverige och USA är liten. Statistik från IARC ger en cancerincidens per 100 000 personer på 547 och 605 för USA respektive Sverige.[7]
Korrektionsfaktorincidens (USA→Sverige): 0,90
Detta ger oss slutligen:
5% ∙ Korr#us ∙ Korrstråldos ∙ Korrålder ∙ Korrincidens =
5% ∙ 0,61 ∙ 0,47 ∙ 1 ∙ 0,9 ≈ 1,3%
Sammantaget ger beräkningen alltså att cirka 1,3% av framtida årliga cancerdiagnoser i Sverige skulle kunna bero på CT-exponering.
—
Stort tack till Christian Göransson, Marcus Söderberg och Patrik Sund som med föredömlig hjälpsamhet bidragit med CT-exponeringsdata från sina regioner.
[1] I inledningen skriver Smith-Bindman att the number of CT examinations ökat >30%, och i diskussionen står det att CT use is 30% higher. Troligtvis avses totalantalet; men även per capita innebär detta en ökning eftersom befolkningen bara vuxit med 8% från 2009 till 2023. (Rapporten som refereras finns ej tillgänglig kostnadsfritt.)
[2] Smith-Bindman skriver att andelen multifas-undersökningar var 28,5%. Vanligtvis används begreppet multi-fas för undersökningar med flera kontrastmedelsfaser, men troligtvis menar Smith-Bindman totala andelen undersökningar med >1 scan eftersom det är detta som är relevant för dosimetrin (samt att metadatan normalt sett inte innehåller information om kontrastmedel explicit). I det svenska material andelen undersökningar med >1 scan 34% (scouter och bolustracking etc exkluderat).
[3] Att överlevnaden är lägre vid 2 år men konvergerar vid 10 år betyder att 2års-överlevarna måste haft en genomsnittligt högre överlevnad än normalt i perioden däremellan. Detta är förmodligen mestadels en depletion of susceptibles-effekt, men det är inte omöjligt att det också finns ett bidrag av socioekonomisk confounding eftersom Mataacs data kommer från ett universitets-/högspecialiserat sjukhus (vilket i USA kan tänkas ha en viss selekterande effekt via försäkringssystemet). Samtidigt kan man också tänka sig att sjukhuset får svårare fall än genomsnittssjukhuset och att dödligheten därför är högre, särskilt initialt. Mataacs data är helt enkelt inte ett idealt jämförelsematerial; men förmodligen ändå det bästa som vi har tillgängligt, och åtminstone bättre än inget.
[4] Låg-, rutin- och högdos-protokollens doser viktades med antalet undersökningar för respektive protokoll.
[5] Smith-Bindman et al. rapporterar för åldrarna 50–59 år en fördelning mellan de fyra kategorierna buk/skalle/thorax/ryggrad på 40%/26%/25%/9%; i det svenska materialet var motsvarande siffror 43%/23%/29%/4%.
[6] Effekten av åldersfördelningen vid exponering kan vi approximera genom att punktvis multiplicera den amerikanska och svenska kurvan med en åldersberoende CT-risk (avläst från Smith-Bindmans Fig. 1) och därefter ta kvoten mellan arean under dessa två kurvor. Detta ger en faktor på 0,8 (alltså 20% färre förväntade fall med svenska fördelningen). Effekten av skillnaden i förväntad livslängd är mer komplicerad att uppskatta. En förenklad (första ordningens) korrektion är att vikta varje punkt med kvoten mellan återstående förväntad livslängd (minus en latenstid på 5 år) via livslängdstabeller för USA och Sverige. Vår kombinerade faktor blir då 0,9. Den sistnämnda korrektionen är dock en underskattning eftersom excess absolut risk ökar med ålder, varför de sista åren skall ha högre vikt. Kurvaturen skulle kunna inkorporeras via BEIR-VII-parametrar i kombination med nationell statistik för åldersberoende grundincidens. Uppskattningsvis skulle korrektionsfaktorn landa i närheten av 1; och att bestämma denna närmre skulle kräva en mer ambitiös modellering än vad som kan motiveras givet arbetsinsatsen och den förmodat försumbara effekten på slutresultatet.
[7] https://gco.iarc.who.int/media/globocan/factsheets/populations (data: 2022; incidence; crude rate; all cancers excl. non-melanoma skin cancer)